|
 |
| J Korean Acad Pediatr Dent > Volume 43(4); 2016 > Article |
|
мҙҲлЎқ
ліё м—°кө¬лҠ” нҳ„мһ¬ мӢңнҢҗлҗҳкі мһҲлҠ” л¶ҲмҶҢ л°”лӢҲмү¬ м ңн’Ҳмқҳ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬ лҠҘл Ҙмқ„ мёЎм •н•ҳкі мқҙмҷҖ н•Ёк»ҳ м •лҹү кҙ‘ нҳ•кҙ‘кё°лҘј мқҙмҡ©н•ҳм—¬ м№ҳм§Ҳмқҳ мһ¬кҙ‘нҷ” нҡЁкіјлҘј 비көҗ, 분м„қн•ҳмҳҖлӢӨ.
нҸүк°Җн•ҳкі мһҗ н•ҳлҠ” л¶ҲмҶҢ л°”лӢҲмү¬лҠ” лӢӨмқҢкіј к°ҷмқҖ 6к°Җм§Җ м ңн’Ҳмқ„ лҢҖмғҒмңјлЎң н•ҳмҳҖлӢӨ; FluoroDoseВ® (FD, Centrix Inc., USA), Enamelastв„ў (EL, Ultradent Product Inc., USA), Clinproв„ў white varnish (CW, 3M ESPE, USA), CavityShieldв„ў (CS, 3M ESPE, USA), V varnishв„ў (VV, Vericom, Korea), MI varnishв„ў (MI, GC, Japan).
MI varnishв„ўмҷҖ V varnishв„ўм—җм„ң лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј мһ¬кҙ‘нҷ”мңЁмқҙ к°ҖмһҘ лҶ’кІҢ лӮҳнғҖлӮң(p < 0.05) л°ҳл©ҙ CS varnishв„ўк°Җ к°ҖмһҘ лӮ®мқҖ лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј мһ¬кҙ‘нҷ”мңЁмқ„ ліҙмҳҖлӢӨ(p < 0.05).
Abstract
Subjects of this study were : FluoroDoseВ® (FD, Centrix Inc., USA), Enamelastв„ў (EL, Ultradent Product Inc., USA), Clinproв„ў white varnish (CW, 3M ESPE, USA), CavityShieldв„ў (CS, 3M ESPE, USA), V varnishв„ў (VV, Vericom, Korea), MI varnishв„ў (MI, GC, Japan).
The amount of fluoride ion release was measured eight times during 168 hours to see change in accumulation with the course of time using a measuring instrument. And the remineralization rate was measured with Quantitative Light-induced Fluorescence (QLF).
V varnishв„ў group and MI varnishв„ў group showed high remineralization rates with statistically significance while CavityShieldв„ў group was the lowest rate of remineralization (p < 0.05).
After that, several chosen samples were scanned through electron microscope (SEM). Demineralized enamel was observed as the number of enamel crystal was very small; enamel rods and crystals were highly protruding. Remineralized groups with fluoride varnishes show the decreasing tendency of the surface roughness compared to the demineralized enamel.
м№ҳм•„мҡ°мӢқмҰқ мҳҲл°©м—җ нҡЁкіјм ҒмңјлЎң м•Ңл Өм ё мһҲлҠ” л¶ҲмҶҢлҠ” лІ•лһ‘м§Ҳмқҳ нғҲнҡҢл°©м§ҖлҠ” л¬јлЎ нғҲнҡҢлҗң лІ•лһ‘м§Ҳмқҳ мһ¬кҙ‘нҷ”м—җ мқҳн•ң м№ҳм§Ҳмқҳ ліөмӣҗмқ„ к°ҖлҠҘн•ҳкІҢ н•ңлӢӨ[1]. м№ҳм•„мҡ°мӢқмҰқ мҳҲл°©мқ„ мң„н•ң л¶ҲмҶҢмқҳ м Ғмҡ©л°©лІ•мқҖ нҒ¬кІҢ м „мӢ м Ғ нҲ¬м—¬л°©лІ•кіј көӯмҶҢм Ғ нҲ¬м—¬л°©лІ•мңјлЎң лӮҳлүҳлҠ”лҚ°, м „мӢ м Ғ нҲ¬м—¬л°©лІ•мқҖ мғҒмҲҳлҸ„мҲҳ л¶ҲмҶҢнҷ”, л¶ҲмҶҢліҙмЎ°м ң ліөмҡ© л“ұмқҙ мһҲмңјл©° көӯмҶҢм Ғ нҲ¬м—¬л°©лІ•мңјлЎңлҠ” л¶ҲмҶҢм№ҳм•Ҫмқҳ мӮ¬мҡ©, л¶ҲмҶҢм–‘м№ҳ, м „л¬ёк°Җл¶ҲмҶҢлҸ„нҸ¬ л“ұмқҙ мһҲлӢӨ.
м „л¬ёк°Җл¶ҲмҶҢлҸ„нҸ¬лІ•мқҖ л¶ҲмҶҢ м Ө(gel), л¶ҲмҶҢ кұ°н’Ҳ(foam), л¶ҲмҶҢ л°”лӢҲмү¬ л“ұ лӢӨм–‘н•ң м ңм ңк°Җ мқҙмҡ©лҗҳкі мһҲлҠ”лҚ° мқҙмӨ‘ л¶ҲмҶҢ л°”лӢҲмү¬к°Җ м•ЎмғҒнҳ•, кұ°н’Ҳнҳ• л“ұкіј 비көҗн•ҳм—¬ л¶Җм°©м„ұмқҙ мўӢкі мӮјнӮ¬ мң„н—ҳм„ұмқҙ м Ғм–ҙ м•Ҳм „н•ҳлӢӨкі м•Ңл Өм ё мһҲлӢӨ[2-5].
л¶ҲмҶҢ л°”лӢҲмү¬лҠ” 1960л…„лҢҖ мӨ‘л°ҳ мң лҹҪм—җм„ң 5% л¶Ҳнҷ”лӮҳнҠёлҘЁмқ„ мЈјм„ұ분мңјлЎң н•ң DuraphatВ® (Colgate-palmolive, USA)мқҙ мӢңнҢҗ лҗң мқҙ лһҳ Fluor ProtectorВ® (Ivoclar-Vivadent, Liechtenstein) л“ұмқҳ 2м„ёлҢҖ л¶ҲмҶҢ л°”лӢҲмү¬л“Өм—җ мқҙм–ҙ к·јлһҳм—җлҠ” Cavity ShieldВ® (Omnii Pharmaceuticals, USA), Vanish AmericaВ® (Dental America, USA) л“ұ мҠӨнӢұнҳ•мқҳ к°ңлі„ нҸ¬мһҘлҗң 3м„ёлҢҖ л°”лӢҲмү¬л“Өмқҙ мӢңнҢҗлҗҳкі мһҲлӢӨ. мөңк·јм—җлҠ” көӯлӮҙм—җм„ңлҸ„ V varnishв„ў (Vericom, Korea) л“ұмқҳ л¶ҲмҶҢ л°”лӢҲмү¬ м ңн’Ҳмқҙ к°ңл°ң, мӢңнҢҗлҗҳкі мһҲлӢӨ.
л¶ҲмҶҢ л°”лӢҲмү¬лҠ” м№ҳм•„м—җ л¶Җм°©м„ұмқҙ мўӢмқҖ мІңм—°мҲҳм§ҖлҘј мЈјм„ұ분мңјлЎң н•ҳкі мһҲм–ҙ 5% л¶Ҳнҷ”лӮҳнҠёлҘЁкіј к°ҷмқҖ кі лҶҚлҸ„мқҳ л¶ҲмҶҢлҘј 비көҗм Ғ мһҘкё°к°„ м№ҳм•„м—җ м ‘мҙүмӢңнӮҙмңјлЎңмҚЁ м№ҳм•„мҡ°мӢқмҰқ мҳҲл°©нҡЁкіјк°Җ мўӢмқҖ кІғмңјлЎң м•Ңл Өм ё мһҲлӢӨ[6,7]. лҳҗн•ң мҲ мӢқмқҙ нҺёлҰ¬н•ҳкі к°„лӢЁн• лҝҗ м•„лӢҲлқј мӢңмҲ мӢңк°„мқҙ 짧아 нҷҳмһҗм—җкІҢ л¶ҖлӢҙмқҙ м ҒмңјлӮҳ л¶ҲмҶҢ л°”лӢҲмү¬ лҳҗн•ң лҸ„нҸ¬ нӣ„ мқјмӢңм Ғмқё м°©мғү, л¶ҲмҫҢн•ң л§ӣ, лҒҲм Ғкұ°лҰ¬лҠ” м§Ҳк°җмңјлЎң мқён•ҙ м–ҙлҰ°мқҙмҷҖ мІӯмҶҢл…„м—җкІҢ лҸ„нҸ¬мӢң кұ°л¶Җк°җмқ„ мӨ„ мҲҳ мһҲмңјл©° мқҢмӢқмқҙлӮҳ нғҖм•Ў, мһҮмҶ”м§Ҳм—җ мқҳн•ҙ м”»кІЁм ё лӮҙл Өк°ҖлҠ” л¬ём ңм җмңјлЎң мқён•ҙ кө¬к°• лӮҙм—җм„ң м Ғм Ҳн•ң л¶ҲмҶҢлҶҚлҸ„лҘј мҳӨлһң мӢңк°„лҸҷм•Ҳ мң м§Җн•ҳлҠ”лҚ° н•ңкі„м җмқ„ к°Җм§Җкі мһҲлӢӨ[8].
мқҙмҷҖ к°ҷмқҖ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ м№ҳм•„мҡ°мӢқмҰқ мҳҲл°© нҡЁкіјм—җ лҢҖн•ң нҳ„мһ¬к№Ңм§Җмқҳ м—°кө¬л“ӨмқҖ мЈјлЎң л¶ҲмҶҢмқҳ лҶҚлҸ„, лҸ„нҸ¬л°©лІ•, лҸ„нҸ¬мЈјкё°м—җ кҙҖн•ң лӮҙмҡ©л“Өмқҙл©°[2,9,10] к·јлһҳм—җлҠ” м ‘м°©л Ҙмқҙ мўӢмқҖ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ л§Өк°ңмІҙм—җ лҢҖн•ң м—°кө¬[11-13]лҸ„ мқҙлЈЁм–ҙм§Җкі мһҲмңјл©° мқҙмҷҖ н•Ёк»ҳ к°Ғмў… мӢңнҢҗ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ нҡЁкіјлӮҳ м„ұлҠҘмқ„ нҸүк°Җн•ҳкё° мң„н•ҙ м—¬лҹ¬ к°Җм§Җ м—°кө¬л“Өмқҙ 진н–үлҗҳм–ҙ мҳӨкі мһҲлӢӨ.
л¶ҲмҶҢ л°”лӢҲмү¬мқҳ нҡЁкіјлӮҳ м„ұлҠҘмқҖ мЈјлЎң л¶ҲмҶҢмқҳ кө¬к°•лӮҙ мһ”лҘҳ мӢңк°„, нғҲнҡҢлҗң мһ¬кҙ‘нҷ” нҡЁкіј л“ұмқ„ 비көҗн•ҳлҠ” кІғмқёлҚ° мқҙлҠ” л¶ҲмҶҢмқҳ м Ғм Ҳн•ң лҶҚлҸ„лӮҳ лҸ„нҸ¬мЈјкё°мҷҖлҸ„ л°Җм ‘н•ҳкІҢ кҙҖл Ёлҗҳм–ҙ мһҲлӢӨ[2,14,15].
Cochrane л“ұ[16]мқҖ лӢӨм„Ҝк°Җм§Җ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ м№јмҠҳкіј л¶ҲмҶҢмқҙмҳЁ л°©м¶ңлҹүмқ„ 비көҗ 분м„қн•ҳмҳҖкі көӯлӮҙ м—°кө¬м—җм„ңлҸ„ мқјл¶Җ мӢңнҢҗ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹү 비көҗм—җ кҙҖн•ң ліҙкі к°Җ мһҲм—Ҳм§Җл§Ң мқҙл“Ө м—°кө¬л“ӨмқҖ лӢЁмҲң л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүл§Ңмқ„ мёЎм •н•ҳмҳҖлӢӨ[17]. мӢӨм ң мһ„мғҒм—җм„ң мӮ¬мҡ©лҗҳлҠ” л¶ҲмҶҢ л°”лӢҲмү¬мқҳ нҡЁлҠҘмқ„ нҸүк°Җн•ҳкё° мң„н•ҙм„ңлҠ” л¶ҲмҶҢмқҙмҳЁ лҶҚлҸ„лҠ” л¬јлЎ мһ¬кҙ‘нҷ” нҡЁкіјлҘј лҸҷмӢңм—җ нҸүк°Җн• н•„мҡ”к°Җ мһҲлҠ”лҚ°, мһ¬кҙ‘нҷ” нҡЁкіјлҠ” л¶ҲмҶҢм„ұ분 мқҙмҷём—җ мІЁк°Җн•ң TCP (Tricalcium phosphate), CPP-ACP (Casein Phosphopeptide- Amorphous Calcium Phosphate) л“ұмқҳ нҡЁкіјк№Ңм§Җ мҙқкҙ„м ҒмңјлЎң нҸүк°Җн• мҲҳ мһҲкё° л•Ңл¬ёмқҙлӢӨ.
кё°мЎҙмқҳ м—°кө¬л“Өм—җм„ң м№ҳм§Ҳмқҳ нғҲнҡҢмҷҖ мһ¬кҙ‘нҷ”лҘј мёЎм •н•ҳлҠ” л°©лІ•мңјлЎңлҠ” нҺёкҙ‘нҳ„лҜёкІҪ, м „мһҗнҳ„лҜёкІҪ, нҡЎлӢЁлҜём„ёл°©мӮ¬м„ лІ•, н‘ңл©ҙлҜём„ёкІҪлҸ„мёЎм • л“ұмқ„ мӮ¬мҡ©н•ҳмҳҖлӢӨ[18-20]. к·ёлҹ¬лӮҳ нҺёкҙ‘нҳ„лҜёкІҪ, м „мһҗнҳ„лҜёкІҪ л“ұмқҖ м •лҹүнҷ” нҸүк°Җк°Җ м–ҙл өкі н‘ңл©ҙлҜём„ёкІҪлҸ„лҠ” мһ¬кҙ‘нҷ”лҗң кө¬мЎ°лҘј ліҙмЎҙн•ҳкё° мң„н•ҙм„ң м—°л§ҲлҘј н•ҳм§Җ м•Ҡкі кҙҖм°°н•ҙм•ј н•ҳлҜҖлЎң мғҒлҢҖм ҒмңјлЎң м •нҷ•м„ұмқҙ л–Ём–ҙ진лӢӨ.
QLF (Quantitative Light-induced Fluorescence)лҠ” м№ҳм§Ҳмқҳ мһ¬кҙ‘нҷ” нҡЁкіјлҘј 비침мҠөм ҒмңјлЎң нҸүк°Җн• мҲҳ мһҲлҠ” кё°кё°лЎң, 405 nm нҢҢмһҘмқҳ н‘ёлҘёмғү к°ҖмӢңкҙ‘м„ мқ„ м№ҳм•„ н‘ңл©ҙм—җ мЎ°мӮ¬н•ҳкі м№ҳл©ҙм—җм„ңмқҳ нҳ•кҙ‘нҳ„мғҒмқ„ мқҙмҡ©н•ҙ[21-23] м№ҳм§Ҳмқҳ нғҲнҡҢм •лҸ„лӮҳ мҙҲкё° м№ҳм•„мҡ°мӢқмҰқмқ„ нғҗм§Җн•ҳкі , м№ҳм§Ҳм—җм„ңмқҳ нҳ•кҙ‘мқҙ мҶҢмӢӨлҗң м •лҸ„лҘј м •лҹүнҷ”мӢңмјң мҙҲкё° м№ҳм•„мҡ°мӢқлі‘мҶҢмқҳ к№ҠмқҙлӮҳ м№ҳм§Ҳмқҳ нғҲнҡҢмҷҖ мһ¬кҙ‘нҷ” м •лҸ„лҘј нҸүк°Җн• мҲҳ мһҲлӢӨ[23,24].
мқҙм „мқҳ м—¬лҹ¬ м—°кө¬л“Ө[25,26]м—җм„ң мӢңнҢҗ мӨ‘мқё мқјл¶Җ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ нҡЁкіјлҘј 비көҗн•ҳкё° мң„н•ҙ л¶ҲмҶҢмқҳ мң лҰ¬ лҠҘл ҘмқҙлӮҳ мһ”лҘҳмӢңк°„мқ„ нҸүк°Җн•ҳкі мһҲм§Җл§Ң, мғқмІҙмӢӨн—ҳмқё кІҪмҡ° м—°кө¬лҢҖмғҒл“Өмқҳ мӢқмҠөкҙҖ, мһҮмҶ”м§Ҳ нҠ№м„ұ, к·ёлҰ¬кі нғҖм•Ў 분비мңЁл“Өмқҙ м„ңлЎң лӢ¬лқј мӢӨн—ҳ лҢҖмғҒмқҳ н‘ңмӨҖнҷ”к°Җ м–ҙл өкі мӢӨн—ҳмӢӨм Ғ мӢӨн—ҳмқҳ кІҪмҡ° нғҖм•Ўмқҳ 분비лЎң мқён•ң л¶ҲмҶҢмқҳ м”»к№Җ л“ұмқҳ кө¬к°•лӮҙ нҷҳкІҪмқ„ мһ¬нҳ„н•ҳм§Җ м•Ҡм•„ 분м„қмқҳ мҳӨм°Ёк°Җ нҒҙ кІғмңјлЎң мӮ¬лЈҢлҗңлӢӨ.
мқҙмҷҖ к°ҷмқҙ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ нҡЁлҠҘм—җ лҢҖн•ң м—¬лҹ¬ м—°кө¬к°Җ 진н–үлҗҳм–ҙ мҳӨкі мһҲмқҢм—җлҸ„ л¶Ҳкө¬н•ҳкі мӢңнҢҗмӨ‘мқё лӢӨм–‘н•ң л¶ҲмҶҢ л°”лӢҲмү¬ м ңн’Ҳм—җ лҢҖн•ң нҡЁкіјлӮҳ м„ұлҠҘм—җ кҙҖн•ҙ 비көҗ, нҸүк°Җн•ң м—°кө¬лҠ” лҜём§„н•ң мӢӨм •мқҙм—¬м„ң мһ„мғҒк°Җл“ӨмқҖ к·јкұ°кё°л°ҳмқҳ л¶ҲмҶҢ л°”лӢҲмү¬ м„ нғқм—җ лҢҖн•ң м •ліҙк°Җ м—¬м „нһҲ л¶ҖмЎұн•ң мғҒнҷ©мқҙлӢӨ. мқҙм—җ ліё м—°кө¬лҠ” нҳ„мһ¬ мӢңнҢҗлҗҳкі мһҲлҠ” л¶ҲмҶҢ л°”лӢҲмү¬ м ңн’Ҳмқҳ нҡЁлҠҘмқ„ ліҙлӢӨ м •нҷ•нһҲ нҸүк°Җн•ҳкё° мң„н•ҙ мӢӨн—ҳмӢӨм ҒмңјлЎң кө¬к°•лӮҙ нғҖм•Ўм—җ мқҳн•ң м”»к№Җнҳ„мғҒмқ„ мһ¬нҳ„н•ҳм—¬ мқҙл“Өмқҳ л¶ҲмҶҢ мң лҰ¬ лҠҘл Ҙмқ„ мёЎм •н•ҳкі мқҙмҷҖ н•Ёк»ҳ QLFлҘј мқҙмҡ©н•ҳм—¬ м№ҳм§Ҳмқҳ мһ¬кҙ‘нҷ” нҡЁкіјлҘј 비көҗ, 분м„қн•ҳкі мһҗ н•ңлӢӨ.
м—°кө¬м—җ мӮ¬мҡ©н•ң л¶ҲмҶҢ л°”лӢҲмү¬лҠ” нҳ„мһ¬ көӯлӮҙм—җм„ң мӢңнҢҗлҗҳкі мһҲлҠ” 6к°Җм§Җ м ңн’Ҳмқ„ лҢҖмғҒмңјлЎң н•ҳмҳҖлӢӨ(Table 1).
мқјнҡҢ мҡ©лҹүмңјлЎң нҸ¬мһҘлҗң м ңн’Ҳмқ„ к°Ғ м ңмЎ°мӮ¬лі„лЎң 20к°ңм”© мӮ¬мҡ©н•ҳмҳҖмңјл©° лӘЁл“ м ңн’ҲмқҖ мӢӨн—ҳ 24мӢңк°„ м „м—җ мғҒмҳЁм—җ ліҙкҙҖн•ң л’Ө лҸ„нҸ¬ м§Ғм „м—җ к°ңлҙүн•ҳм—¬ мӮ¬мҡ©н•ҳмҳҖлӢӨ.
м ңн’ҲлӢ№ 10 mgмқҳ л°”лӢҲмү¬лҘј 5 Г— 5 mmлЎң м ҲлӢЁн•ң мҶҢмқҳ м№ҳм•„ н‘ңл©ҙм—җ л§ҲмқҙнҒ¬лЎңлёҢлҹ¬мү¬лҘј мқҙмҡ©н•ҳм—¬ лҸ„нҸ¬н•ҳмҳҖлӢӨ. л°”лӢҲмү¬лҘј лҸ„нҸ¬н•ң мӢңнҺёмқҖ 20 mLмқҳ мқёкіө нғҖм•Ў(мҰқлҘҳмҲҳ + 1.5 mM Ca(No3)2вҲҷ4H2O + 0.9 mM NaH2PO4вҲҷ2H2O + 150 mM KCl + 0.1 mM Tris buffer + 0.03 ppm F, pH 7.0, 37в„ғ)м—җ м№Ём ҒмӢңнӮЁ нӣ„ 37в„ғ н•ӯмҳЁкё°м—җ ліҙкҙҖн•ҳмҳҖлӢӨ.
мқёкіөнғҖм•Ўм—җ мң лҰ¬лҗң л¶ҲмҶҢмқҙмҳЁмқҳ лҶҚлҸ„лҠ” 1мӢңк°„, 2мӢңк°„, 4мӢңк°„, 8мӢңк°„, 24мӢңк°„, 72мӢңк°„, 168мӢңк°„ л“ұ мҙқ 8нҡҢ мёЎм •н•ҳмҳҖмңјл©° мқёкіө нғҖм•ЎмқҖ л§Ө 3мӢңк°„л§ҲлӢӨ мҙқлҹүмқҳ 1/2мқ„ мғҲлЎң көҗнҷҳн•ҙ мЈјм—ҲлӢӨ.
л§Ө мёЎм • мӢңк°„л§ҲлӢӨ л¶ҲмҶҢ л°”лӢҲмү¬лҘј лҸ„нҸ¬н•ң мӢңнҺёмқҙ ліҙкҙҖлҗң мқёкіө нғҖм•Ў 20 mLм—җм„ң 0.5 mLлҘј 분лҰ¬н•ҳм—¬ л¶ҲмҶҢмқҙмҳЁ лҶҚлҸ„лҘј мёЎм •н•ҳмҳҖлӢӨ.
л¶ҲмҶҢмқҙмҳЁм „к·№(Orion 9609, Thermo Scientific, USA)мқҳ ліҙм •мқ„ мң„н•ҙ 10 ppm, 1 ppm, 0.1 ppm, 0.01 ppmмқҳ л¶ҲмҶҢ н‘ңмӨҖ мҡ©м•Ўмқ„ мӮ¬мҡ©н–ҲлӢӨ. мӨҖ비лҗң л¶ҲмҶҢ н‘ңмӨҖмҡ©м•Ў 5 mLмҷҖ TISAB III (Total Ionic Strength Buffer III) 0.5 mLлҘј 10:1мқҳ л¶Җ피비лЎң нҳјн•©н•ҳмҳҖлӢӨ.
л¶ҲмҶҢмқҙмҳЁм „к·№мқ„ л¶ҲмҶҢмқҙмҳЁмёЎм •кё°(Orion 4-star, Thermo Scientific, USA)м—җ м—°кІ°н•ҳкі лӮ®мқҖ лҶҚлҸ„мқҳ н‘ңмӨҖмҡ©м•Ўл¶Җн„° мҲңм„ңлҢҖлЎң ліҙм •н•ҳм—¬ кё°мӨҖк°’мқ„ л¶ҲмҶҢмқҙмҳЁмёЎм •кё°м—җ мһ…л Ҙн•ҳмҳҖлӢӨ. л¶ҲмҶҢлҶҚлҸ„лҠ” л¶ҲмҶҢмқҙмҳЁмёЎм •кё°м—җ м ңмЎ°мӮ¬мқҳ м§ҖмӢңм—җ л”°лқј л¶ҲмҶҢмқҙмҳЁм „к·№мқ„ л¶Җм°©н•ҳкі л¶ҲмҶҢ н‘ңмӨҖмҡ©м•ЎмңјлЎң кё°кё°мқҳ н‘ңмӨҖнҷ”лҘј мӢңн–үн•ң лӢӨмқҢ мёЎм •н•ҳмҳҖлӢӨ. м „к·№мқҳ м „мң„к°Җ мҳЁлҸ„м—җ мқҳн•ҙ ліҖнҷ”лҗҳлҠ” кІғмқ„ л°©м§Җн•ҳкё° мң„н•ҳм—¬ мҲҳ집н•ң лӘЁл“ мқёкіөнғҖм•Ў н‘ңліёкіј н‘ңмӨҖмҡ©м•Ўмқ„ 25в„ғмқҳ лҸҷмқјн•ң мҳЁлҸ„м—җм„ң мёЎм •н–ҲлӢӨ. 10к°ңмқҳ мӢңнҺёмқ„ мёЎм •н• л•Ңл§ҲлӢӨ кё°кё°мқҳ н‘ңмӨҖнҷ”лҘј мӢңн–үн•ҳмҳҖмңјл©° лӘЁл“ мёЎм •мқҖ м„ё лІҲ мёЎм •н•ҳкі н‘ңмӨҖм •лҹүмқ„ мң„н•ҙ м„ё лІҲм§ё к°’мқ„ м„ нғқн•ҳмҳҖлӢӨ.
л°ңкұ°лҗң мҶҢмқҳ м Ҳм№ҳ мӨ‘ нҢҢм Ҳмқҙ м—Ҷкі , кұҙм „н•ң лІ•лһ‘м§Ҳ н‘ңл©ҙмқ„ к°–лҠ” м№ҳм•„лҘј лҢҖмғҒмңјлЎң мӢңнҺёмқ„ м ңмһ‘н•ҳмҳҖлӢӨ. мҶҢмқҳ м Ҳм№ҳлҘј м ҖмҶҚн•ёл“ңн”јмҠӨлЎң 6 mm Г— 3 mm Г— 3 mmмқҳ нҒ¬кё°лЎң м ҲлӢЁн•ң нӣ„ лҜёлҰ¬ м ңмһ‘лҗң м•„нҒ¬лҰҙ мЈјнҳ•м—җ л§ӨлӘ°н•ҳмҳҖлӢӨ. л§ӨлӘ°лҗң мӢңнҺёмқ„ silicon carbamide paperлҘј мқҙмҡ©н•ҳм—¬ 400, 800, 2400 к·ёлҰ¬кі 4000 gritк№Ңм§Җ лӢЁкі„м ҒмңјлЎң м—°л§Ҳн•ҳмҳҖлӢӨ. м—°л§Ҳ нӣ„ мӢңнҺё н‘ңл©ҙм Ғмқҳ 1/2мқё 3 mm Г— 3 mmм—җ nail varnishлҘј лҸ„нҸ¬н•ҳмҳҖлӢӨ.
мҙҲкё° мҡ°мӢқлі‘мҶҢ мғқм„ұмқ„ мң„н•ң нғҲнҡҢ мҡ©м•ЎмқҖ 2.2 mM Ca(NO3)2, 2.2 mM KHxPO4, acetic acid 50 mMмқ„ 2м°Ё мҰқлҘҳмҲҳм—җ нҳјн•©н•ҳм—¬ pH 4.5лЎң мЎ°м Ҳн•ҳм—¬ м ңмһ‘н•ҳмҳҖлӢӨ. мӢңнҺёмқ„ нғҲнҡҢ мҡ©м•Ўм—җ 37в„ғлЎң 72мӢңк°„ лҸҷм•Ҳ ліҙкҙҖн•ҳм—¬ мҙҲкё° мҡ°мӢқмқ„ мң л°ңн•ҳмҳҖмңјл©° нғҲнҡҢ мҡ©м•ЎмқҖ 24мӢңк°„ л§ҲлӢӨ көҗмІҙн•ҳмҳҖлӢӨ.
нғҲнҡҢлҗң мӢңнҺёл“Өмқ„ QLF-D (QLF-D biluminatorв„ў, Inspektor Research system BV, Amsterdam, The Netherlands)лҘј мқҙмҡ©н•ҳм—¬ нғҲнҡҢ м •лҸ„мқё QLFмқҳ в–іF к°’мқ„ мёЎм •н•ҳмҳҖлӢӨ(Fig. 1). мӢңнҺёмқҳ в–іF к°’мқҙ мҙҲкё° м№ҳм•„мҡ°мӢқмҰқмқ„ мқҳлҜён•ҳлҠ”, -25 - -15 лІ”мң„лҘј к°–лҠ” 120к°ңлҘј м„ нғқн•ң нӣ„ мқҙ мӢңнҺёл“Өмқ„ л¬ҙмһ‘мң„лЎң 20к°ңм”© 6к°ңмқҳ кө°мңјлЎң 배분н•ҳмҳҖлӢӨ.
к°Ғ мӢңнҺёмқҳ нғҲнҡҢлҗң л¶Җ분м—җ л¶ҲмҶҢ л°”лӢҲмү¬лҘј м „мҡ© м–ҙн”ҢлҰ¬мјҖмқҙн„°лҘј мқҙмҡ©н•ҳм—¬ лҸ„нҸ¬ нӣ„ 30분 лҸҷм•Ҳ кұҙмЎ°н•ҳмҳҖлӢӨ. мқёкіө нғҖм•Ўм—җ лӢҙк·ј мӢңнҺёмқ„ 37в„ғ н•ӯмҳЁкё°м—җ ліҙкҙҖн•ҳмҳҖлӢӨ. 6мӢңк°„ л’Ө м–ҙлҰ°мқҙмҡ© 칫мҶ”лЎң лӮЁмқҖ л¶ҲмҶҢлҘј м ңкұ°н•ҳкі мқёкіө нғҖм•Ўмқ„ көҗнҷҳн•ҳм—¬ 37в„ғ н•ӯмҳЁкё°м—җ ліҙкҙҖн•ҳмҳҖлӢӨ. мӢңнҺёмқ„ мқёкіө нғҖм•Ўм—җ 1мЈјмқј лҸҷм•Ҳ мң„м№ҳмӢңмј°мңјл©° мқёкіө нғҖм•ЎмқҖ 6мӢңк°„л§ҲлӢӨ көҗмІҙн•ҳмҳҖлӢӨ.
QLF-DлҘј мқҙмҡ©н•ҳм—¬ мӢңнҺёл“Өмқҳ в–іF к°’мқ„ лҸҷмқјн•ң мӢӨн—ҳмһҗк°Җ м•”мӢӨм—җм„ң мёЎм •н•ҳмҳҖлӢӨ. QLF-D мҳҒмғҒмқҖ л””м§Җн„ё м№ҙл©”лқј(EOS-550D, Canon, Tokyo, Japan)лЎң м…”н„° мҠӨн”јл“ң 1/45мҙҲ, мЎ°лҰ¬к°ңк°’ 3.2 к·ёлҰ¬кі ISO 1600мңјлЎң м„Өм •н•ҳм—¬ мҙ¬мҳҒн•ҳмҳҖлӢӨ. м»ҙн“Ён„° мһҗлҸҷ м ҖмһҘ мҶҢн”„нҠёмӣЁм–ҙлЎң C3 v1.18 (Inspektor Research System BV)мқ„, 분м„қ н”„лЎңк·ёлһЁмңјлЎң QA v1.18 (Inspektor Research System BV)мқ„ мӮ¬мҡ©н•ҳмҳҖлӢӨ. QLF-DлЎң мёЎм •н•ң в–іFк°’мқҳ мһ¬кҙ‘нҷ”мңЁ(нҡҢліөлҘ )мқҖ лӢӨмқҢмқҳ кіөмӢқмңјлЎң кө¬н•ҳмҳҖлӢӨ.
лІ•лһ‘м§Ҳ н‘ңл©ҙмқҳ лҜём„ёкө¬мЎ° 분м„қмқ„ мң„н•ҙ мЈјмӮ¬м „мһҗнҳ„лҜёкІҪ(JEOL JSM-840A, JEOL CO., Japan)мқ„ мқҙмҡ©н•ҳмҳҖлӢӨ. мӢңнҺёл“Өмқ„ 진кіө лҚ°мӢңкІҢмқҙн„°лҘј мқҙмҡ©н•ҳм—¬ 충분нһҲ кұҙмЎ°мӢңмјңмӨҖ лӢӨмқҢ Ion sputter (E-1030, Hitachi, Japan)лҘј мқҙмҡ©н•ҳм—¬ л°ұкёҲ мҪ”нҢ…мқ„ 80мҙҲ к°„ мӢңн–үн•ҳмҳҖлӢӨ. н‘ңл©ҙмқҙ мҪ”нҢ…лҗң мӢңнҺёмқ„ м№ҙліён…Ңмқҙн”„лҘј мқҙмҡ©н•ҳм—¬ мӢңлЈҢлҢҖ мң„м—җ мһҘм°©н•ң нӣ„ мЈјмӮ¬м „мһҗнҳ„лҜёкІҪмңјлЎң 10000л°°м—җм„ң кҙҖм°°н•ҳмҳҖлӢӨ.
мӢңк°„м—җ л”°лҘё лҲ„м Ғлҗң л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқ„ нҸүк°Җн•ҳкё° мң„н•ҙм„ң Kruskal-Wallis testлҘј мӢңн–үн•ҳмҳҖлӢӨ. нғҲнҡҢмҷҖ мһ¬кҙ‘нҷ” м •лҸ„лҘј Wilcoxon matched-pairs signed ranks testлҘј мӮ¬мҡ©н•ҳм—¬ 분м„қн•ҳмҳҖлӢӨ. нғҲнҡҢ нӣ„ л¶ҲмҶҢ л°”лӢҲмү¬ мў…лҘҳм—җ л”°лҘё кө° к°„ мһ¬кҙ‘нҷ”мқҳ мң мқҳм„ұ м°ЁмқҙлҘј 비көҗн•ҳкё° мң„н•ҙ мӮ¬нӣ„ кІҖм •мңјлЎң Mann Whitney U-testлҘј мӢңн–үн•ҳмҳҖлӢӨ. к·ёлҰ¬кі л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј лІ•лһ‘м§Ҳ мһ¬кҙ‘нҷ”мқҳ мғҒкҙҖкҙҖкі„лҘј м•Ңм•„ліҙкё° мң„н•ҙм„ң SpearmanвҖҷs correlation analysisлҘј мӢңн–үн•ҳмҳҖлӢӨ.
мҙқ 168мӢңк°„ лҸҷм•Ҳмқҳ мӢңк°„ кІҪкіјм—җ л”°лқј 8нҡҢ мёЎм •лҗң лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҖ к°Ғ л¶ҲмҶҢ л°”лӢҲмү¬ к·ёлЈ№л“Ө к°„м—җ м„ңлЎң мң мқҳн•ң м°ЁмқҙлҘј ліҙмҳҖмңјл©°(p < 0.05), мөңмў… мёЎм • мӢңк°„мқё 168мӢңк°„ кІҪкіјмӢң мёЎм •н•ң лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҖ MI к·ёлЈ№кіј VV к·ёлЈ№м—җм„ң мң мқҳн•ҳкІҢ лҶ’м•ҳкі EL, CP, FD к·ёлЈ№ мҲңмқҙм—ҲлӢӨ. CS к·ёлЈ№мқҙ нҶөкі„м ҒмңјлЎң мң мқҳн•ҳкІҢ к°ҖмһҘ лӮ®мқҖ лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқ„ ліҙмҳҖлӢӨ(p < 0.05, Fig. 2).
лҸ„нҸ¬ нӣ„ 10мӢңк°„ мқҙлӮҙмқҳ кІҪмҡ° VV к·ёлЈ№кіј MI к·ёлЈ№мқҳ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҖ лӢӨлҘё к·ёлЈ№л“Өм—җ 비н•ҙм„ң мӣ”л“ұнһҲ лҶ’м•ҳм§Җл§Ң(p < 0.05) мӢңк°„мқҙ м§ҖлӮ мҲҳлЎқ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҠҘл Ҙмқҙ к°җмҶҢн•ҳлҠ” м–‘мғҒмқ„ ліҙм—¬мӨҖ л°ҳл©ҙ лӢӨлҘё к·ёлЈ№мқҳ л¶ҲмҶҢ л°”лӢҲмү¬л“ӨмқҖ 168мӢңк°„ к№Ңм§Җ мң лҰ¬лҠҘл Ҙмқҙ мғҒлҢҖм ҒмңјлЎң л§Һмқҙ к°җмҶҢн•ҳм§Җ м•Ҡм•ҳлӢӨ(Fig. 3). к·ёлҹ¬лӮҳ к°Ғ мёЎм • кё°к°„лҸҷм•Ҳ VV к·ёлЈ№кіј MI к·ёлЈ№мқҙ мғҒлҢҖм ҒмңјлЎң лҚ” л§ҺмқҖ л¶ҲмҶҢмқҙмҳЁмқ„ мң лҰ¬н•ҳмҳҖлӢӨ. EL к·ёлЈ№мқҖ нҠ№мқҙн•ҳкІҢ мӢңк°„мқҙ кІҪкіјн• мҲҳлЎқ лҚ” л§ҺмқҖ л¶ҲмҶҢмқҙмҳЁмқ„ л°©м¶ңн•ҳлҠ” нҳ„мғҒмқ„ ліҙмҳҖлӢӨ.
лӘЁл“ л¶ҲмҶҢ л°”лӢҲмү¬ к·ёлЈ№м—җм„ң нғҲнҡҢлҗң мӢңнҺёмқҳ л¶ҲмҶҢ л°”лӢҲмү¬ лҸ„нҸ¬ нӣ„мқҳ мһ¬кҙ‘нҷ”мңЁ(RО”F)мқҖ нҶөкі„м ҒмңјлЎң мң мқҳн•ң м°ЁмқҙлҘј лӮҳнғҖлғҲлӢӨ(p < 0.05, Table 2).
VV к·ёлЈ№кіј MI к·ёлЈ№мқҖ лӢӨлҘё к·ёлЈ№л“Өм—җ 비н•ҙм„ң нҶөкі„м ҒмңјлЎң мң мқҳн•ҳкІҢ лҶ’мқҖ мһ¬кҙ‘нҷ”мңЁмқ„ ліҙм—¬мЈјм—Ҳмңјл©°, CS к·ёлЈ№мқҖ нҶөкі„м ҒмңјлЎң к°ҖмһҘ лӮ®мқҖ мһ¬кҙ‘нҷ”мңЁмқ„ ліҙм—¬мЈјм—ҲлӢӨ(p < 0.05, Table 3).
Fig. 4лҠ” нғҲнҡҢлҗң лІ•лһ‘м§Ҳкіј к°Ғк°Ғ лӢӨлҘё л¶ҲмҶҢ л°”лӢҲмү¬лҘј м Ғмҡ©н•ҳм—¬ мһ¬кҙ‘нҷ”лҗң к·ёлЈ№л“Өмқҳ лҢҖн‘ңм Ғмқё мЈјмӮ¬м „мһҗнҳ„лҜёкІҪ мҶҢкІ¬мқҙлӢӨ. нғҲнҡҢлҗң лІ•лһ‘м§ҲмқҖ мЈјнҢҢм„ мЎ°(perikymata)лҘј л”°лқј лІ•лһ‘мҶҢмЈј(enamel prism)мқҳ л§җлӢЁл¶Җк°Җ н•ЁлӘ°лҗң нҳ•нғңлЎң нҢҢкҙҙлҗң м–‘мғҒмқ„ ліҙмқҙл©° мқҙмҷём—җлҸ„ 집мҶҢкіө(focal hole) л“ұмқҙ л¶Җ분м ҒмңјлЎң кҙҖм°°лҗҳм—ҲлӢӨ. л¶ҲмҶҢ л°”лӢҲмү¬лҘј м Ғмҡ©н•ҳм—¬ мһ¬кҙ‘нҷ”лҗң к·ёлЈ№л“ӨмқҖ нғҲнҡҢлҗң лІ•лһ‘м§Ҳм—җ 비н•ҳм—¬ н‘ңл©ҙ кұ°м№ кё°к°Җ к°җмҶҢн•ң м–‘мғҒмқ„ ліҙм—¬ м№ҳм§Ҳмқҳ нҡҢліөмқҙ мғҒлӢ№нһҲ мқҙлЈЁм–ҙ진 м–‘мғҒмқ„ ліҙмқҙкі мһҲлӢӨ. Enamelastв„ў, Clinpro White varnishв„ў, CavityShieldв„ў к·ёлЈ№мқҖ мһ¬кҙ‘нҷ”лҗң лІ•лһ‘м§Ҳ н‘ңл©ҙм—җ лҜём„ёкіө(micropore)кіј лҜём„ёк· м—ҙмқҙ кҙҖм°°лҗҳм—Ҳмңјл©° лӢӨлҘё л¶ҲмҶҢ л°”лӢҲмү¬ к·ёлЈ№м—җ 비н•ҳм—¬ лІ•лһ‘м§Ҳ н‘ңл©ҙмқҙ лҚ” л¶Ҳк·ңм№ҷн•ҳмҳҖкі FluoroDoseВ®, MI varnishв„ў, V varnishв„ў к·ёлЈ№мқҖ мғҒлҢҖм ҒмңјлЎң лҚ” л§ӨлҒ„лҹ¬мҡҙ (smooth) н‘ңл©ҙмқ„ ліҙмқҙкі мһҲлӢӨ(Fig. 4).
FluoroDoseВ® к·ёлЈ№кіј Clinpro White varnishв„ў к·ёлЈ№мқ„ м ңмҷён•ң лӘЁл“ л¶ҲмҶҢ л°”лӢҲмү¬ к·ёлЈ№л“Өмқҳ 168мӢңк°„к№Ңм§Җ лҲ„м Ғлҗң л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҳ мҲңм„ңлҠ” лҢҖл¶Җ분 лІ•лһ‘м§Ҳ мһ¬кҙ‘нҷ”мңЁмқҳ мҲңм„ңмҷҖ мқјм№ҳн•ҳмҳҖлӢӨ. лҲ„м Ғлҗң л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј лІ•лһ‘м§Ҳ мһ¬кҙ‘нҷ”мқҳ мғҒкҙҖкҙҖкі„ 분м„қм—җм„ң л§Өмҡ° лҶ’мқҖ мғҒкҙҖкі„мҲҳ(Оі=0.89)лҘј ліҙмҳҖкі л”°лқјм„ң лҶ’мқҖ м–‘мқҳ мғҒкҙҖкҙҖкі„к°Җ мһҲмқҢмқ„ м•Ң мҲҳ мһҲм—ҲлӢӨ.
лӢӨлҘё көӯмҶҢм Ғ л¶ҲмҶҢлҸ„нҸ¬ м ңм ңмҷҖ лҢҖ비лҗҳлҠ” л¶ҲмҶҢ л°”лӢҲмү¬мқҳ лҢҖн‘ңм Ғмқё мһҘм җмқҖ кө¬к°• лӮҙ лҸ„нҸ¬ нӣ„, мқјм • кё°к°„ лҸҷм•Ҳ м§ҖмҶҚм ҒмңјлЎң л¶ҲмҶҢк°Җ кө¬к°• лӮҙм—җ мң лҰ¬лҗЁмңјлЎңмҚЁ м№ҳм•„мқҳ мһ¬кҙ‘нҷ”лҘј мҙү진мӢңнӮӨлҠ” кІғмқҙлӢӨ. 비лЎқ лҢҖл¶Җ분мқҳ м ңн’Ҳл“Өмқҙ лҸҷмқјн•ң лҶҚлҸ„мқҳ л¶ҲмҶҢнҷ”н•©л¬ј(5% NaF)лҘј н•Ёмң н•ҳкі мһҲм§Җл§Ң, м ңн’Ҳл§ҲлӢӨ л¬јм„ұкіј кө¬м„ұ м„ұ분мқҙ лӢӨлҘҙкё° л•Ңл¬ём—җ к°Ғ м ңн’Ҳ к°„ н•ӯмҡ°мӢқ л°Ҹ мһ¬кҙ‘нҷ” лҠҘл Ҙмқҳ м°Ёмқҙк°Җ мЎҙмһ¬н• кІғмқҙлӢӨ. л¶ҲмҶҢ л°”лӢҲмү¬мқҳ кө¬к°• лӮҙ л¶ҲмҶҢмқҙмҳЁмқҳ лҶҚлҸ„мҷҖ л¶ҲмҶҢмқҳ мһ”лҘҳ мӢңк°„мқҖ мқјм°Ём ҒмңјлЎң мҡҙл°ҳл§Өк°ңмІҙм—җ н•Ёмң лҗң л¶ҲмҶҢлҹүм—җ мқҳн•ҙ мҳҒн–Ҙмқ„ л°ӣм§Җл§Ң к·ё мҷём—җлҸ„ л§Өк°ңмІҙмқҳ л¬јлҰ¬нҷ”н•ҷм Ғ м„ұм§Ҳм—җлҸ„ мҳҒн–Ҙмқ„ л°ӣмқ„ мҲҳ мһҲлӢӨ.
л¶ҲмҶҢ л°”лӢҲмү¬ к·ёлЈ№л“Өмқҳ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқ„ лҲ„м ҒмңјлЎң 168мӢңк°„ мқҙнӣ„ мёЎм •н•ң кІ°кіј MI varnishв„ўмҷҖ V varnishв„ўм—җм„ң мң мқҳн•ҳкІҢ лҶ’мқҖ к°’мқҙ мёЎм •лҗҳм—Ҳкі , CavityShieldв„ўк°Җ нҶөкі„м ҒмңјлЎң мң мқҳн•ҳкІҢ к°ҖмһҘ лӮ®мқҖ л¶ҲмҶҢмқҙмҳЁ лҲ„м Ғ мң лҰ¬лҹүмқ„ ліҙмҳҖлҠ”лҚ° мқҙлҠ” к°ҷмқҖ м–‘мқҳ NaFлҘј н•Ёмң н•ҳкі мһҲлӢӨкі н•ҳлҚ”лқјлҸ„ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ м„ұ분мқҙлӮҳ л¬јлҰ¬нҷ”н•ҷм Ғ м„ұмғҒм—җ л”°лқј л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ лӢ¬лқјм§Ҳ мҲҳ мһҲмқҢмқ„ мқҳлҜён•ңлӢӨ.
л¶ҲмҶҢ л°”лӢҲмү¬лҠ” мЈјлЎң мҶЎм§„, shellac, colophonium л“ұ мІңм—°л Ҳ진мқ„ нҸ¬н•Ён•ң л Ҳ진과 urethane methacrylate л“ұмқҳ кі л¶„мһҗк°Җ мЈјм„ұ분мқҙл©° м—¬кё°м—җ м•ҢмҪ”мҳ¬мқҙлӮҳ м—җнғ„мҳ¬ л“ұмқҳ мҡ©м ң, л¶Ҳнҷ”лӮҳнҠёлҘЁ(sodium fluoride), мғүмҶҢ(colorant), н–ҘлҜёлЈҢ(flavorant), к·ёлҰ¬кі м ‘м°©л Ҙмқ„ лҶ’мқҙкё° мң„н•ң м җм°©м ң(adherent) л“ұмқ„ мІЁк°Җн•ңлӢӨ. лҢҖл¶Җ분мқҳ л¶ҲмҶҢ л°”лӢҲмү¬ м ңм ңлҠ” 5% NaF, мҰү 1 mL мҡ©л§Өм—җ 50 mgмқҳ л¶ҲмҶҢлҘј мІЁк°Җн•ҳм—¬ 22.6 mgмқҳ л¶ҲмҶҢмқҙмҳЁм—җ мғҒмқ‘н•ҳлҠ” м–‘мқ„ н•Ёмң н•ҳкі мһҲм§Җл§Ң мөңк·јм—җлҠ” л¶ҲмҶҢ л°”лӢҲмү¬мқҳ м№ҳм•„мҡ°мӢқмҰқ мҳҲл°©нҡЁкіј нҳ№мқҖ мһ¬кҙ‘нҷ” нҡЁкіјлҘј мҰқк°ҖмӢңнӮӨкё° мң„н•ҙ xylitolмқҙлӮҳ TCP, CPP-ACP л“ұмқ„ 추к°ҖлЎң мІЁк°Җн•ҳкё°лҸ„ н•ңлӢӨ[27-30]. MI varnishв„ўлҠ” CPP-ACPлҘј, V varnishв„ўлҠ” TCP, Rosin, Xylitolмқ„ н•Ёмң н•ҳкі мһҲлӢӨ. мқҙмҷҖ к°ҷмқҖ лӢӨлҘё мЈјм„ұ분м—җ мқҳн•ҙм„ң л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҳ м°Ёмқҙк°Җ л°ңмғқн• мҲҳ мһҲлӢӨкі мғқк°ҒлҗңлӢӨ.
л¶ҲмҶҢ л°”лӢҲмү¬мқҳ м№ҳм•„мҡ°мӢқмҰқ мҳҲл°© нҡЁкіјлҘј нҸүк°Җн•ҳкё° мң„н•ҙ л§ҺмқҖ м—°кө¬л“Өмқҙ ліҙкі лҗҳм–ҙмҷ”лӢӨ. Ritwik л“ұ[31]мқҖ 5% NaFлҘј н•Ёмң н•ҳлҠ” л„Ө мў…лҘҳмқҳ л¶ҲмҶҢ л°”лӢҲмү¬мқё Premier Enamel Provarnishв„ў, Colgate PreviDentв„ў, Omni varnishв„ў, Omni Varnish XTTMлҘј к°Ғк°Ғ л°ңкұ°лҗң м№ҳм•„м—җ м Ғмҡ©н•ҳмҳҖкі мқёкіө нғҖм•Ўм—җ лӢҙк·ј нӣ„ л¶ҲмҶҢ л°©м¶ңлҹүмқ„ 48мӢңк°„ лҸҷм•Ҳ мёЎм •н•ҳмҳҖлӢӨ. к·ё кІ°кіјм—җм„ң Premier Enamel Provarnishв„ўк°Җ к°ҖмһҘ л§ҺмқҖ л¶ҲмҶҢмқҙмҳЁмқ„ мң лҰ¬н•ҳм—¬ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ м ңн’Ҳм—җ л”°лқј м°Ёмқҙк°Җ мһҲмқҢмқ„ м ңмӢңн•ҳкё°лҸ„ н•ҳмҳҖлӢӨ.
л¶ҲмҶҢмқҙмҳЁмқҳ мң лҰ¬лҹүмқҖ л¶ҲмҶҢ л°”лӢҲмү¬ м ңм ңмқҳ м„ұ분мқҖ л¬јлЎ мқҙкі л¬јлҰ¬нҷ”н•ҷм Ғ нҠ№м„ұ, мҰү м№ҳл©ҙм—җм„ңмқҳ м –мқҢм„ұ(wetability), м ‘м°©л Ҙ, мҡ©л§Өмқҳ нңҳл°ңм„ұ л“ұмқҙ мў…н•©м ҒмңјлЎң кҙҖл Ёлҗҳм–ҙ мһҲлӢӨ. л”°лқјм„ң к°ҷмқҖ л¶ҲмҶҢ н•Ёмң лҹүмқ„ к°Җм§Җкі мһҲм–ҙлҸ„ мң„мҷҖ к°ҷмқҖ л¬јлҰ¬нҷ”н•ҷм Ғ нҠ№м„ұмқҳ м°ЁмқҙлЎң мқён•ҙ л¶ҲмҶҢмқҙмҳЁмқҳ мң лҰ¬лҹүмқҙ лӢӨлҘј мҲҳ мһҲлӢӨ.
мқҙмҷҖ к°ҷмқҖ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҠҘл Ҙмқ„ нҸүк°Җн• л•Ң мӮ¬лһҢмқ„ лҢҖмғҒмңјлЎң н•ң кІҪмҡ° мӢқмқҙмҠөкҙҖ, мһҮмҶ”м§Ҳ мҠөкҙҖ, нғҖм•Ўмқҳ м җлҸ„мҷҖ 분비лҹүм—җ л”°лқј л¶ҲмҶҢ л°”лӢҲмү¬мқҳ кө¬к°•лӮҙ л¶Җм°©лҠҘкіј м”»к№Җнҳ„мғҒм—җ лҢҖн•ң к°ңмқёлӢ№ нҺём°Ёк°Җ м»Өм„ң м •нҷ•н•ң 비көҗк°Җ м–ҙл Өмҡё кІғмңјлЎң мғқк°ҒлҗңлӢӨ. ліё м—°кө¬лҠ” мӢӨн—ҳмӢӨм Ғмқё м—°кө¬лЎң мһ¬кҙ‘нҷ” м •лҸ„к°Җ 비мҠ·н•ң мӢңнҺёмқ„ м–»кё° мң„н•ҙ мҶҢмқҳ м№ҳм•„лҘј мӮ¬мҡ©н•ҳмҳҖмңјл©° л¶ҲмҶҢмқҙмҳЁмқ„ мёЎм •н•ҳлҠ” кіјм •м—җм„ң л¶ҲмҶҢл°”лӢҲмү¬к°Җ лҸ„нҸ¬лҗң мӢңнҺёмқҙ лӢҙкёҙ мқёкіөнғҖм•Ўмқ„ л§Ө 3мӢңк°„л§ҲлӢӨ 1/2м”© көҗмІҙн•ЁмңјлЎңмҚЁ мӢӨм ң кө¬к°•нҷҳкІҪмқ„ мһ¬нҳ„н•ҳкі мһҗ л…ёл Ҙн•ҳмҳҖлӢӨ.
мқҙ мӢӨн—ҳмқҖ 168мӢңк°„лҸҷм•Ҳмқҳ л¶ҲмҶҢмқҙмҳЁ л…ём¶ңлҹүмқ„ лҲ„м ҒмӢңнӮЁ кІ°кіјлЎңмҚЁ л¶ҲмҶҢмқҙмҳЁмқҳ мҙҲкё° мң лҰ¬лҹүкіј нӣ„кё° мң лҰ¬лҹүмқҖ к°Ғк°Ғмқҳ л¶ҲмҶҢ л°”лӢҲмү¬ м ңм ңм—җ л”°лқјм„ң м°Ёмқҙк°Җ мһҲм—ҲлӢӨ. V varnishв„ўлҠ” к°ҖмһҘ лҶ’мқҖ мһ¬кҙ‘нҷ”мңЁмқ„ ліҙм—¬мЈјм—Ҳкі л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүлҸ„ л‘җ лІҲм§ёлЎң лҶ’м•ҳм§Җл§Ң мӢңк°„мқҙ м§ҖлӮ мҲҳлЎқ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ л–Ём–ҙмЎҢкі , MI varnishв„ўлҠ” м§ҖмҶҚм Ғмқё л¶ҲмҶҢмқҙмҳЁ мң лҰ¬ нҡЁкіјлҘј ліҙм—¬мЈјм—ҲлӢӨ. к·ёлҹ¬лӮҳ м—¬м „нһҲ V varnishв„ўмҷҖ MI varnishв„ўк°Җ лҶ’мқҖ мқҙмҳЁ лҶҚлҸ„лҘј ліҙм—¬мЈјкі мһҲлӢӨ. Enamelastв„ўлҠ” 17мӢңк°„ мқҙнӣ„м—җ л§Ө мёЎм • мӢңм җм—җм„ң л¶ҲмҶҢмқҙмҳЁлҶҚлҸ„к°Җ V varnishв„ўлӮҳ MI varnishв„ўліҙлӢӨ лҶ’кІҢ лӮҳнғҖлӮҳ м§ҖмҶҚм Ғмқё мң лҰ¬лҠҘл Ҙмқҙ л§Өмҡ° мҡ°мҲҳн•Ёмқ„ ліҙм—¬мЈјкі мһҲлӢӨ. м•һмңјлЎң мқјм • кё°к°„ лҸҷм•Ҳ мң лҰ¬н•ң м „мІҙ л¶ҲмҶҢмқҙмҳЁлҹүмқҙ л§ҺмқҖ кІҪмҡ°к°Җ лҚ” нҡЁкіјм Ғмқём§Җ нҳ№мқҖ м§ҖмҶҚм ҒмңјлЎң мң лҰ¬н•ҳлҠ” лҠҘл Ҙмқҙ лҚ” нҡЁкіјм Ғмқём§Җм—җ лҢҖн•ҙм„ңлҠ” лҚ” л§ҺмқҖ м—°кө¬к°Җ н•„мҡ”н•ҳлӢӨкі мғқк°ҒлҗңлӢӨ. мһҘкё°к°„мқҳ мӢӨн—ҳмқ„ нҶөн•ң мһ¬кҙ‘нҷ”мқҳ мёЎм •мқҖ л¶ҲмҶҢ л°”лӢҲмү¬мқҳ м§ҖмҶҚм Ғмқё л¶ҲмҶҢмқҙмҳЁмқҳ мң лҰ¬лҠҘл Ҙмқҳ нҸүк°ҖлҘј к°ҖлҠҘн•ҳкІҢ н• кІғмқҙлӢӨ.
мқҙ м—°кө¬м—җм„ңлҠ” л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹү лҝҗ м•„лӢҲлқј л¶ҲмҶҢ л°”лӢҲмү¬мқҳ мһ¬кҙ‘нҷ” лҠҘл ҘлҸ„ лҸҷмӢңм—җ нҸүк°Җн•ҳмҳҖлӢӨ. к·ёлҰ¬н•ҳм—¬ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј л¶ҲмҶҢ л°”лӢҲмү¬м—җ мқҳн•ң лІ•лһ‘м§Ҳмқҳ мһ¬кҙ‘нҷ” лҠҘл Ҙмқҳ мғҒкҙҖкҙҖкі„лҘј ліј мҲҳ мһҲм—ҲлӢӨ. лҲ„м Ғлҗң л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј лІ•лһ‘м§Ҳ мһ¬кҙ‘нҷ”мқҳ мғҒкҙҖкҙҖкі„ 분м„қм—җм„ң лҶ’мқҖ м–‘мқҳ мғҒкҙҖкҙҖкі„к°Җ мһҲм—ҲлӢӨ. 비лЎқ FluoroDoseTMмҷҖ Clinpro White varnishв„ўмқҳ мһ¬кҙ‘нҷ”мңЁмқҙ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҳ мҲңм„ңмҷҖ м°Ёмқҙк°Җ мһҲм—Ҳм§Җл§Ң л‘җ к·ёлЈ№к°„мқҳ мһ¬кҙ‘нҷ”мңЁм—җ нҶөкі„м ҒмңјлЎң мң мқҳн•ң м°Ёмқҙк°Җ мЎҙмһ¬н•ҳм§Җ м•Ҡм•ҳкё° л•Ңл¬ём—җ 충분нһҲ л°ӣм•„л“Өмқјл§Ңн•ң кІ°кіјлқјкі 여겨진лӢӨ.
л¶ҲмҶҢ л°”лӢҲмү¬мқҳ мһ¬кҙ‘нҷ” лҠҘл Ҙмқ„ мёЎм •н•ҳкё° мң„н•ҙ ліё м—°кө¬лҠ” QLFлҘј мқҙмҡ©н•ҳмҳҖлҠ”лҚ° мқҙлҠ” QLFк°Җ нҳ„мһ¬ м—¬лҹ¬ л¬ён—Ңл“Өм—җ мқҳн•ҙ к·ё мӢ лў°м„ұмқҙ лҶ’кі , нҠ№нһҲ көҗн•©л©ҙ мҡ°мӢқмҰқм—җм„ң лӢӨлҘё 진лӢЁ л°©лІ•л“Өм—җ 비н•ҙ мўӢмқҖ 진лӢЁ лҠҘл Ҙмқ„ к°–кі мһҲкё° л•Ңл¬ёмқҙлӢӨ[32,33].
лҳҗн•ң лІ•лһ‘м§Ҳмқҳ нғҲнҡҢмҷҖ мһ¬кҙ‘нҷ”лҘј нҸүк°Җн• мҲҳ мһҲлҠ” м—¬лҹ¬ к°Җм§Җ л°©лІ•л“Ө мӨ‘, мӢңнҺёмқҳ нғҲнҡҢ м „нӣ„ н‘ңл©ҙлҜём„ёкІҪлҸ„ мёЎм •мқҙлӮҳ нҺёкҙ‘нҳ„лҜёкІҪ, м „мһҗнҳ„лҜёкІҪ л“ұмқ„ мқҙмҡ©н•ң кҙҖм°°мқҖ мёЎм • л¶Җмң„лҘј м •нҷ•нһҲ лӢӨмӢң мһ¬нҳ„н• мҲҳ м—ҶлҠ”лҚ° л°ҳн•ҙ QLFлҠ” мқҙм „ мҙ¬мҳҒмқҙ мһ¬нҳ„ к°ҖлҠҘн•ҳлӢӨлҠ” мһҘм җмқҙ мһҲлӢӨ. к°Ғ мӢңнҺёл“Өмқҳ нғҲнҡҢ мқҙм „мқҳ QLF мҙ¬мҳҒкіј мһ¬кҙ‘нҷ” мқҙнӣ„мқҳ QLF мҙ¬мҳҒмқҖ 99%мқҳ мһ¬нҳ„м„ұмңјлЎң мӨ‘мІ©(repositioning)лҗҳм—ҲлӢӨ. мқҙлҹ° лҶ’мқҖ мһ¬нҳ„м„ұмңјлЎң мқён•ҙм„ң QLF О”F к°’мқҳ ліҖнҷ”лЎң м–»м–ҙм§ҖлҠ” мһ¬кҙ‘нҷ”мңЁм—җ мӢ лў°м„ұмқ„ л¶Җм—¬н•ҳмҳҖлӢӨ.
л¶ҲмҶҢ л°”лӢҲмү¬м—җ мқҳн•ҙ мһ¬кҙ‘нҷ”лҗң н‘ңл©ҙмқ„ кҙҖм°°н•ҳкё° мң„н•ҙ мЈјмӮ¬м „мһҗнҳ„лҜёкІҪмқ„ мқҙмҡ©н•ң лІ•лһ‘м§Ҳ н‘ңл©ҙкө¬мЎ°лҘј мҙ¬мҳҒн•ҳмҳҖлӢӨ. мһ¬кҙ‘нҷ”лҗң лІ•лһ‘м§Ҳ н‘ңл©ҙм–‘мғҒмқ„ нҸүк°Җн•ҳкё° мң„н•ҙ нғҲнҡҢлҗң лІ•лһ‘м§ҲмқҖ лҢҖмЎ°кө°мңјлЎңм„ң мӮ¬мҡ©лҗҳм—ҲлӢӨ. л¶ҲмҶҢ л°”лӢҲмү¬лҘј м Ғмҡ©н•ҳм—¬ 168мӢңк°„лҸҷм•Ҳ мһ¬кҙ‘нҷ”лҗң к·ёлЈ№л“ӨмқҖ лҢҖмЎ°кө°мқё нғҲнҡҢлҗң лІ•лһ‘м§Ҳм—җ 비н•ҙ л§ӨлҒҲн•ң лІ•лһ‘м§Ҳ н‘ңл©ҙкіј л§ҺмқҖ лІ•лһ‘м§Ҳ кІ°м •, к·ёлҰ¬кі лІ•лһ‘мҶҢмЈјкіөк°„мқҳ 축мҶҢ л“ұмқҙ кҙҖм°°лҗңлӢӨ. л¶ҲмҶҢ л°”лӢҲмү¬к°Җ м Ғмҡ©лҗң к·ёлЈ№л“Ө мӨ‘ CavityShieldв„ўлҠ” лӢӨлҘё л¶ҲмҶҢ л°”лӢҲмү¬м—җ 비н•ҳм—¬ лІ•лһ‘м§Ҳ н‘ңл©ҙмқҙ л¶Ҳк·ңм№ҷн•ҳм—¬ лІ•лһ‘мҶҢмЈјк°Җ лҲҲм—җ лқ„лҠ” м–‘мғҒмқҙ кҙҖм°°лҗҳм—Ҳкі , V varnishв„ў, MI varnishв„ўлҠ” мғҒлҢҖм ҒмңјлЎң л§ӨлҒҲн•ң н‘ңл©ҙмқ„ ліҙм—¬мЈјм—ҲлҠ”лҚ° мқҙлҠ” мқҙ л‘җ л¶ҲмҶҢ л°”лӢҲмү¬ к·ёлЈ№мқҙ лҚ” лӣ°м–ҙлӮң мһ¬кҙ‘нҷ” нҡЁкіјлҘј ліҙм—¬ н‘ңл©ҙ кұ°м№ кё°к°Җ к°җмҶҢн•ҳмҳҖкё° л•Ңл¬ёмңјлЎң мғқк°ҒлҗңлӢӨ.
ліё м—°кө¬лҠ” л¶ҲмҶҢ л°”лӢҲмү¬мқҳ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј мһ¬кҙ‘нҷ”мңЁмқҳ мғҒкҙҖкҙҖкі„лҘј лҸ„м¶ңн•ҳмҳҖлӢӨ. 비лЎқ 7мқјмқҙлқјлҠ” лӢЁкё°к°„мқҳ мӢӨн—ҳмқҙм—Ҳм§Җл§Ң мӢңмӨ‘м—җм„ң нҢҗл§Өлҗҳкі мһҲлҠ” 6к°Җм§Җмқҳ л¶ҲмҶҢ л°”лӢҲмү¬лҘј мӢӨн—ҳн•ҳмҳҖмңјл©°, л¶ҲмҶҢ л°”лӢҲмү¬мқҳ мһ¬кҙ‘нҷ” нҡЁкіјм—җ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ лҜём№ҳлҠ” мҳҒн–Ҙмқ„ нҸүк°Җн• мҲҳ мһҲм—ҲлӢӨ. м•һмңјлЎң мһҘкё°к°„мқҳ м—°кө¬лҠ” мӢңк°„м—җ л”°лҘё л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ мһ¬кҙ‘нҷ”м—җ лҜём№ҳлҠ” мҳҒн–ҘлҸ„ нҸүк°Җн• мҲҳ мһҲмқ„ кІғмқҙлӢӨ.
MI varnishв„ўмҷҖ V varnishв„ўм—җм„ң лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ к°ҖмһҘ лҶ’мқҖ(p < 0.05) л°ҳл©ҙ CS varnishв„ўк°Җ к°ҖмһҘ лӮ®мқҖ лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқ„ ліҙмҳҖлӢӨ(p < 0.05).
V varnishв„ўмҷҖ MI varnishв„ўм—җм„ң мҙҲкё°мқҳ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ мӣ”л“ұнһҲ лҶ’м•ҳкі мӢңк°„мқҙ м§ҖлӮ мҲҳлЎқ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ к°җмҶҢн•ҳлҠ” м–‘мғҒмқ„ ліҙмҳҖмңјлӮҳ лӢӨлҘё л¶ҲмҶҢ м ңм ңлҠ” мӢңк°„ кІҪкіјм—җ л”°лҘё л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқҙ мғҒлҢҖм ҒмңјлЎң лҚң к°җмҶҢн•ҳмҳҖлӢӨ. к·ёлҹ¬лӮҳ к°Ғ мёЎм •мӢңкё°м—җм„ң V varnishв„ўмҷҖ MI varnishв„ўк°Җ лӢӨлҘё л¶ҲмҶҢ л°”лӢҲмү¬ м ңм ңм—җ 비н•ҙ лҚ” л§ҺмқҖ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүмқ„ ліҙмҳҖлӢӨ.
лӘЁл“ л¶ҲмҶҢ л°”лӢҲмү¬ к·ёлЈ№м—җм„ң нғҲнҡҢ лІ•лһ‘м§Ҳ мӢңнҺёмқҳ л¶ҲмҶҢ лҸ„нҸ¬ нӣ„ О”Fк°’мқҖ нҶөкі„м ҒмңјлЎң мң мқҳн•ҳкІҢ мҰқк°Җн•ҳмҳҖлӢӨ. нғҲнҡҢлҗң лІ•лһ‘м§Ҳмқҳ мһ¬кҙ‘нҷ”мңЁмқҖ V varnishв„ў, MI varnishв„ўк°Җ к°ҖмһҘ лҶ’м•ҳмңјл©°(p < 0.05) CS varnishв„ўк°Җ к°ҖмһҘ лӮ®м•ҳлӢӨ(p < 0.05). EL, FD, CP varnishв„ўк°„мқҳ мһ¬кҙ‘нҷ”мңЁмқҳ м°ЁмқҙлҠ” м—Ҷм—ҲлӢӨ.
мЈјмӮ¬м „мһҗнҳ„лҜёкІҪмқ„ мқҙмҡ©н•ң лІ•лһ‘м§Ҳ н‘ңл©ҙкө¬мЎ°м—җм„ң л¶ҲмҶҢ л°”лӢҲмү¬лҘј м Ғмҡ©н•ҳм—¬ мһ¬кҙ‘нҷ”лҗң к·ёлЈ№л“ӨмқҖ нғҲнҡҢлҗң лІ•лһ‘м§Ҳм—җ 비н•ҳм—¬ н•ЁлӘ°лҗң лІ•лһ‘мҶҢмЈјк°Җ нҡҢліөлҗң м–‘мғҒмқ„ ліҙмҳҖмңјл©° мқҙмӨ‘ V varnishв„ўмҷҖ MI varnishв„ўк°Җ лӢӨлҘё м ңм ңм—җ 비н•ҳм—¬ лҚ” л§ӨлҒҲн•ң н‘ңл©ҙмқ„ ліҙмҳҖлӢӨ.
лҲ„м Ғ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј лІ•лһ‘м§Ҳ мһ¬кҙ‘нҷ”лҠ” л§Өмҡ° лҶ’мқҖ мғҒкҙҖкі„мҲҳ(0.89)лҘј ліҙмқҙлҠ” м–‘мқҳ мғҒкҙҖкҙҖкі„к°Җ мһҲм—ҲлӢӨ(p < 0.05).
мқҙмғҒмқҳ кІ°кіјлҘј мў…н•©н•ҙ ліҙл©ҙ ліё м—°кө¬м—җм„ңлҠ” V varnishв„ўмҷҖ MI varnishв„ўк°Җ к°ҖмһҘ лҶ’мқҖ л¶ҲмҶҢмқҙмҳЁ мң лҰ¬лҹүкіј мһ¬кҙ‘нҷ” нҡЁкіјлҘј лӮҳнғҖлғҲлӢӨ.
Fig.В 2.
Changes of cumulative fluoride concentration release (ppm) from the various fluoride varnishes according to the test time. FD : FluoroDoseВ®, EL : Enamelastв„ў, CP : Clinpro White varnishв„ў, CS : CavityShieldв„ў, VV : V varnishв„ў, MI : MI varnishв„ў
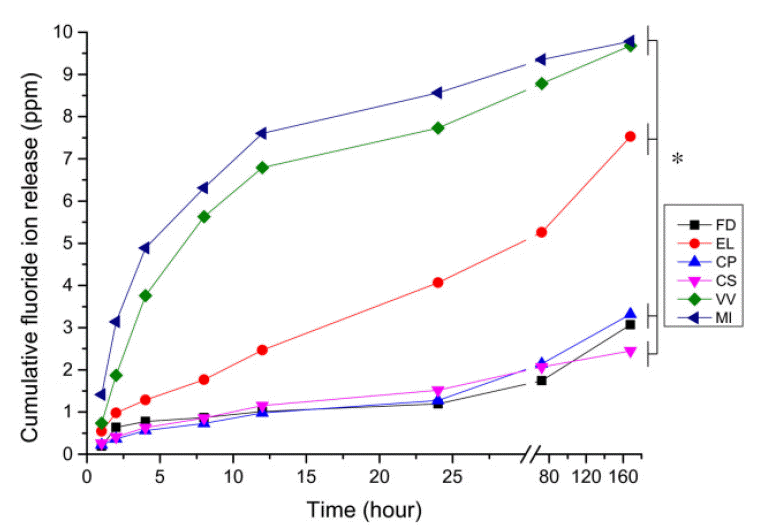
Fig.В 4.
The scanning electron microscope images of the enamel surfaces in each groups (Г—10000). (A) Demineralization surface presents partial dissolution of enamel prism and shows increasing amount of craters. Interrod and intercrystal spaces of enamel are prominent; (B) Enamelastв„ў, (C) Clinpro White varnishв„ў, (D) CavityShieldв„ў. And (E) FluoroDoseВ®, (F) MI varnishв„ў, (G) V varnishв„ў groups show more smooth surfaces than other groups.

TableВ 1.
Fluoride varnish products used in this study
TableВ 2.
Recovery percentage of each groups
| Demineralization (О”F, Mean +/- SD) | After treatment (О”F, Mean +/- SD) | RО”F (%, Mean +/- SD) | |
|---|---|---|---|
| VV | -18.31 Вұ 2.79 | -8.70 Вұ 2.91 | 47.44 Вұ 20.50* |
| MI | -19.41 Вұ 3.13 | -9.84 Вұ 3.06 | 52.95 Вұ 12.64* |
| EL | -20.34 Вұ 3.60 | -12.34 Вұ 1.98 | 37.79 Вұ 13.22* |
| FD | -23.56 Вұ 2.00 | -16.35 Вұ 3.42 | 30.75 Вұ 13.11* |
| CP | -21.38 Вұ 2.99 | -15.73 Вұ 3.09 | 26.38 Вұ 11.45* |
| CS | -20.56 Вұ 2.23 | -17.98 Вұ 1.98 | 12.29 Вұ 6.49* |
References
2. BeltraвҖІn-Aguilar ED, Goldstein JW, Lockwood SA : Fluoride varnishes. J Am Dent Assoc, 131:589-96, 2000.


3. White DJ, Nelson DGA, Faller RV : Mode of action of fluoride: application of new techniques and test methods to the examination of the mechanism of action of topical fluoride. Advances in Dental Research, 8:166-174, 1994.


4. вҲ…gaard B, SeppГӨ L, Rolla G : Professional topical fluoride applications -clinical efficacy and mechanism of action. Adv Dent Res. 8:190-201, 1994.


5. Mohammadi TM, Hajizamani A, Hajizamani HR, Abolghasemi B : Fluoride Varnish Effect on Preventing Dental Caries in a Sample of 3-6 Years Old Children. J Int Oral Health. 7:30-35, 2015.
6. Fejerskov O, Thylstrup A, Larsen MJ : Rational use of fluorides in caries prevention. Acta Odontol Scand, 39:241-249, 1981.


7. Ten Cate JM : In vitro studies on the effects of fluoride on de- and remineralization. J Dent Res. 69:614-619, 1990.


8. Munshi AK, Reddy NN, Shetty V : A comparative evaluation of three fluoride varnishes : an in-vitro. J Indian Soc Pedod Prev Dent, 19:92-102, 2001.

9. Hodgson BD : An alternative technique for applying fluoride varnish. J Am Dent Assoc, 136:1295-1297, 2005.


10. Adair SM : Current fluoride therapy in dentistry for children. Current Opinion Dent, 1:583-591, 1991.
11. Kim MJ, Lee SH, Lee NY, Lee IH : Evaluation of the effect of PVA tape supplemented with 2.26% fluoride on enamel demineralization using microhardness assessment and scanning electron microscopy: in vitro study. Arch Oral Biol, 58:160-166, 2013.


12. Im SO, Lee SH, Lee NY, Park SH : The Fluoride releasing effect of PVA fluoride-polymer adhesive tape. J Korean Acad Pediatr Dent, 38:327-336, 2011.

13. Jih MK, Lee SH, Lee NY : Effect of polymer adhesive film supplemented 5% NaF on enamel remineralization. J Korean Acad Pediatr Dent, 41:218-224, 2014.

14. Hazelrigg CO, Dean JA, Fontana M : Fluoride varnish concentration gradient and its effect on enamel demineralization. Pediatr Dent, 25:119-126, 2003.

15. Petersson LG, Twetman S, Lingström P : Professional fluoride varnish treatment for caries control: a systematic review of clinical trials. Acta Odontol Scand, 62:170-176, 2004.


16. Cochrane NJ, Shen P, Yuan Y, Reynolds EC : Ion release from calcium and fluoride containing dental varnishes. Aust Dent J, 59:100-105, 2014.


17. Kim HN, Jeong MS, Jeong SH, et al. : Evaluation of release of fluoride from dental varnishes marked in Korea. J Korean Acad Oral Health, 38:131-137, 2014.

18. Toumba KJ, Curzon ME : A clinical trial of a slowreleasing fluoride device on children. Caries Res, 39:195-200, 2005.


19. Marini I, Cecchi L, Vecchiet F, et al. : Intraoral fluoride releasing device: a new clinical therapy for dentine sensitivity. J Periodontol, 71:90-95, 2000.


20. Zero DT, Fu J, Espeland MA, et al. : Comparison of fluoride concentrations in unstimulated whole saliva following use of a fluoride dentifrice and a fluoride rinse. J Dent Res, 67:1257-1262, 1988.


22. Retief DH, Summerlin DJ, Harris BE, et al. : An evaluation of three procedures for fluoride analysis. Caries Res, 19:248-254, 1985.


23. Front MS, Ross JW jr : Use of total ionic strength adjustment buffer for electrode determination of fluoride in water supplies. Anal Chem, 40:1169-1171, 1968.


24. Edelstein BL, Cottrel D, O sullivan D, et al. : Comparison of colorimeter and electrode analysis of water fluoride. Pediatr Dent, 14:47-49, 1992.

25. Weinberger SJ, Johnston DW, Wright GZ : A comparison of two systems for measuring water fluoride ion level. Clin Prev Dent, 11:19-22, 1989.

26. Ritwik P, Aubel JD, Hagan J : Evaluation of short-term fluoride release from fluoride varnishes. J Clin Pediatr Dent, 36:275-278, 2012.


27. Alamoudi SA, Pani SC, Alomari M : The effect of the addition of tricalcium phosphate to 5% sodium fluoride varnishes on the microhardness of enamel of primary teeth. Int J Dent, 2013:486358, 2013.



28. Tabrizi A, Cakirer B : A comparative evaluation of casein phosphopeptide-amorphous calcium phosphate and fluoride on the shear bond strength of orthodontic brackets. Eur J Orthod, 33:282-287, 2011.


29. Huang GJ, Roloff-Chiang B, Matunas JC, et al. : Effectiveness of MI Paste Plus and PreviDent fluoride varnish for treatment of white spot lesions: a randomized controlled trial. Am J Orthod Dentofacial Orthop, 143:31-41, 2013.



30. Pereira Ade F, Silva TC, Buzalaf MA, et al. : Xylitol concentrations in artificial saliva after application of different xylitol dental varnishes. J Appl Oral Sci, 20:146-150, 2012.



- TOOLS
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 5,949 View
- 182 Download
- Related articles






 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print